Tomografía de Coherencia Óptica: papila y capa de fibras nerviosas
Dres. Mingo Botín D, Blázquez Escudero G, Cabrejas Martínez L, Guerrero Altares L
Hospital Universitario Ramón y Cajal. Madrid.
Bases de la OCT
El funcionamiento de la tomografía de coherencia óptica (OCT) es comparable al de un ecógrafo, con la particularidad de utilizar luz en lugar de ultrasonidos. El aparato emite un haz de luz monocromática (820 nm), y un divisor de haces lo separa en dos, que son enviados a un espejo de referencia y al ojo. La interferencia de los dos haces reflejados es procesada por un interferómetro. De este modo, la distancia de las estructuras se mide por el tiempo de retraso de la luz reflejada, y la intensidad de la señal, dependiente de las propiedades ópticas del tejido, se transforma en una escala logarítmica de falsos colores. Los colores «cálidos» (blanco, rojo) indican alta reflectividad, y los «fríos» (negro, azul) representan reflectividad baja. Así se obtienen imágenes pseudohistológicas, a un nivel de resolución en torno a las 10 µ.
Como principales ventajas destacan su rapidez, inocuidad, ausencia de contacto, buena reproductibilidad y alta resolución. Asimismo, no requiere plano de referencia y no es afectada por la birrefringencia de los medios. Su mayor inconveniente es la necesidad de transparencia de medios, por tratarse de un sistema óptico, así como de una mínima colaboración por parte del paciente.
Protocolos de exploración
Respecto a la OCT aplicada a la papila, existen varios patrones de adquisición de imágenes disponibles en el Stratus OCT (Carl Zeiss Meditec Inc., Dublin, CA), probablemente el modelo más difundido en la actualidad. Éstos incluyen líneas radiales a través del centro del disco óptico, así como rastreos (scans) circunferenciales a través de la capa de fibras nerviosas de la retina peripapilar. El usuario puede elegir entre la adquisición de imágenes individuales, o seleccionar protocolos más rápidos, que realizan automáticamente múltiples rastreos, aunque con una menor resolución transversal.
- Capa de fibras nerviosas (CFN): se utilizan principalmente dos protocolos de exploración, ambos con círculo de 3,46 mm de diámetro que el explorador centra en la papila. El RNLF thickness hace 512 scans en una sola línea, y el Fast RNFL thickness hace directamente 3 líneas de 256 scans cada una en 1,92 segundos.
- Disco óptico: estos protocolos realizan 6 líneas radiales de 4mm a través de la papila, bien de una en una con 512 scans por línea (Optic disc), o bien 6 líneas consecutivas de 128 scans en 1,92 segundos (Fast Optic disc).
Protocolos de análisis
La OCT utiliza algoritmos automáticos basados en las propiedades ópticas de los tejidos para poder realizar mediciones sobre las imágenes obtenidas. La CFN es altamente reflectante por la disposición de sus fibras perpendicular al haz de luz. Así, en los exámenes de la CFN, puede determinar su espesor considerando la distancia entre su límite posterior y la interfase vitreorretinana. En el caso del disco óptico, tomando como referencias la superficie anterior de la CFN y el límite del epitelio pigmentario peripapilar, realiza un análisis topográfico de la cabeza del nervio óptico.
Por otro lado, existen varios índices de calidad del examen que deben ser tenidos en cuenta a la hora de la interpretación. Estos incluyen signal to noise ratio (SNR), que debe tener un mínimo de 30dB, un porcentaje de scans aceptados mínimo del 90%, y una intensidad de la señal (signal strenght) mayor de 5 sobre 10.
Capa de fibras nerviosas
Stratus OCT dispone de 5 tipos de análisis de la CFN. El más sencillo, RNFL Thickness, muestra las medidas de la CFN en cada uno de los cortes obtenidos. Otros dos tratan de analizar el cambio entre diferentes exámenes: RNFL Thickness Serial Analysis compara gráficamente hasta cuatro exámenes de cada ojo, y RNFL Thickness Change muestra el cambio entre dos exámenes de cada ojo de forma tanto gráfica como numérica.
El protocolo más utilizado, RNFL Thickness Average, muestra el grosor a lo largo de la CFN de cada ojo, la comparación gráfica entre ambos ojos, y los valores numéricos por cuadrantes y sectores horarios (fig. 1). Además, aporta una base normativa que compara los datos con la población normal de la misma edad, clasificándolos en percentiles asociados a colores. Blanco indica valores esperados en más del 95%, verde entre el 5 y 95% (normal), amarillo del 1 al 5% (limítrofe), y rojo por debajo del 1% (fuera de límites normales). Hay que tener en cuenta que no existe base normativa para menores de 18 años, y que en la comparación se valora la edad, pero no otros parámetros como la raza, el tamaño de la papila ni la longitud axial, que también afectan al espesor de la CFN. Tampoco debemos olvidar que, según esta categorización, un 5% (1 de cada 20) de sujetos normales serían clasificados fuera del color verde.
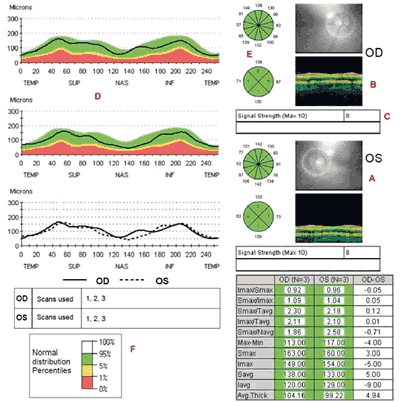
Fig. 1. Hoja de resultados RNFL Thickness Average. Se observa el centrado correcto del círculo de exploración en la imagen de fondo (A), buena delimitación de la CFN (B) y signal strenght superior a 5 (C). Tanto el perfil de espesor del corte explorado (D), como el grosor por sectores horarios y cuadrantes (E) están dentro de la normalidad (F).
Muchos estudios han indagado la capacidad de la OCT para diferenciar sujetos normales y glaucomatosos, arrojando cifras de sensibilidad del 61 al 84%, y especificidad del 85 al 90%. Estas dependen de los parámetros y criterios elegidos, resultando la mejor curva ROC (relación entre S y E) para el espesor medio (0,96) y el del cuadrante inferior (0,97), seguidos por el superior (0,95) (1).
Por otro lado, la OCT puede tener una gran utilidad en el diagnóstico precoz y de progresión del glaucoma, ya que los cambios estructurales preceden, a veces mucho tiempo, a los perimétricos. Aunque no existe un sistema de análisis de progresión por software en OCT, probablemente por el rápido avance de esta tecnología frente a los plazos necesarios para su estudio, si investigaciones al respecto. Así, se ha correlacionado cada estadio glaucomatoso con un grosor de la CFN (2) y se ha mostrado como una herramienta prometedora en el diagnóstico del glaucoma preperimétrico (3). Para determinar cuánto cambio puede considerarse progresión debemos conocer la reproductibilidad de las medidas, que se ha cifrado entorno a las 10 µ para el espesor medio (4). Sin embargo, aún existen muchos factores que introducen variabilidad, aumentada en especial a menor intensidad de señal y a menor grosor medio de la CFN, por lo que es más difícil establecer cambios cuando los medios no son transparentes o en glaucomas avanzados (5). El tamaño y morfología del disco, la longitud axial y el grupo étnico son otros factores que también afectan a las medidas.
Disco óptico
El protocolo de análisis Optic Nerve Head reproduce una imagen topográfica aproximada de la papila, sobre la que realiza diferentes mediciones anatómicas en el corte seleccionado (diámetro de disco y de excavación, anchura del anillo, etc) y de la integración de los 6 cortes (área y volumen del anillo, razón E/P horizontal y vertical, entre otros). Los parámetros más significativos para su uso en glaucoma han resultado la relación de área excavación/disco y el área del anillo. Sin embargo, este protocolo ha resultado menos útil en su aplicación al glaucoma al no existir una base normativa morfométrica, mostrar menor reproductibilidad y grados bajos de acuerdo con la exploración clínica (6) y otras técnicas de imagen como la fotografía estereoscópica y el HRT (7).
Otras aplicaciones
Son muchos los estudios llevados a cabo en otros campos, especialmente en el de la Neurooftalmología. Así, se ha visto cómo la OCT puede ser un biomarcador de actividad y progresión de las neuropatías desmielinizantes (h). En la neuropatía óptica isquémica anterior no arterítica se ha demostrado que existe una menor relación excavación/disco (E/P), pero no un disco más pequeño, y se han correlacionado los parámetros de OCT con la pérdida visual y campimétrica. También ha mostrado su utilidad en el seguimiento del papiledema y las drusas del nervio óptico, en el diagnóstico precoz de neuropatías tóxicas y nutricionales, y un valor pronóstico en las neuropatías compresivas. En definitiva, se trata de una técnica de imagen de alta precisión que hace posible un estudio estructural de la CFN y el disco óptico.
OCT de alta definición
La nueva generación de OCT, también conocida como de dominio espectral o de Fourier, aporta como principal innovación una velocidad de adquisición de A-scans 70 veces más rápida. El Cirrus OCT (Carl Zeiss Meditec Inc., Dublin, CA), para el análisis de la papila examina un cubo de 200x200 líneas en 1,6 segundos con una resolución en torno a las 5 µ. De este cubo extrae 256 puntos a lo largo del círculo de cálculo de 3,46 mm, centrado automáticamente en la papila, que componen la imagen tomográfica. A diferencia de su predecesor, permite modificar la posición de la papila y los limites anterior y posterior de la CFN si el observador considera que son erróneos.
El informe Optic disc cube 200x200 incluye, además del espesor medio y la representación por cuadrantes y sectores horarios, un parámetro de simetría entre ambos ojos, que también se compara con una base normativa. También presenta Mapas de grosor, que imitan el patrón de color de GDx, con colores fríos (azul, verde) para las áreas más delgadas, y colores calidos (amarillo, rojo) para las áreas más gruesas. Y por último, en los Mapas de desviación superpone a la imagen del fondo de ojo píxeles rojos (1%) o amarillos (5%) que vienen de la comparación con la base de normalidad. El mayor automatismo y resolución de esta nueva generación probablemente deriven en una mayor capacidad diagnóstica y de seguimiento, que deberá ser probada en nuevos estudios.
Bibliografía
- Budenz DL, Michael A,Chang RT, McSoley J,Katz J. Sensitivity and Specificity of the StratusOCT for Perimetric Glaucoma. Ophthalmology 2005; 112: 3-9.
- Sihota R, Sony P, Gupta V, Dada T, Singh R. Diagnostic Capability of Optical Coherence Tomography in Evaluating the Degree of Glaucomatous Retinal Nerve Fiber Damage. Invest Ophthalmol Vis Sci 2006; 47: 2006-2010
- Mayoral F, Polo V, Ferreras A, Larrosa JM, Pueyo V, Honrubia F. Capacidad diagnóstica del Stratus OCT para detectar glaucomas pre-perimétricos. Arch Soc Esp Oftalmol 2006; 81: 537-544.
- Budenz DL, Fredette MJ,Feuer WJ,Anderson DR. Reproducibility of Peripapillary Retinal Nerve Fiber Thickness Measurements with Stratus OCT in Glaucomatous Eyes. Ophthalmology 2008; 115: 661-666.
- Wu Z, Vazeen M,Varma R,Chopra V,Walsh AC,LaBree LD, et al. Factors Associated with Variability in Retinal Nerve Fiber Layer Thickness Measurements Obtained by Optical Coherence Tomography. Ophthalmology 2007; 114: 1505-1512.
- Arnalich-Montiel F, Muñoz-Negrete FJ, Rebolleda G, Sales-Sanz M, Cabarga C. Cup-to-disc ratio: agreement between slit-lamp indirect ophthalmoscopic estimation and stratus optical coherence tomography measurement. Eye 2007; 21: 1041-1049.
- Barkana Y, Harizman N, Gerber Y, Liebmann JM, Ritch R. Measurements of optic disk size with HRT II, Stratus OCT, and funduscopy are not are not interchangeable. Am J Ophthalmol 2006; 142: 375-80.