Diagnóstico y manejo de las metástasis de coroides
J Donate1,6, L López Guajardo2,6, R Abreu3,6, R Gallego4,6, R Dolz5,6
1 Hospital Clínico Universitario San Carlos. Madrid.
2 Hospital Universitario Príncipe de Asturias.
3 Hospital Uniersitario Viergen de la Candelaria. Sta Cruz de Tenerife.
4 Hospital Universitario y Politécnico La Fe. Valencia.
5 Vitreous Retina Macula Consultants, Nueva York (EEUU).
6 Club Español de la Mácula.
Introducción
La coroides como tejido altamente vascularizado constituye una red que fácilmente se convierte en objetivo de patologías a distancia, como embolismos sépticos o no, o implantación a distancia de células tumorales desde otras localizaciones. La primera metástasis coroidea documentada data de 1872 por Perls y se cuenta con que hasta el 8% de los fallecidos por enfermedad tumoral maligna tienen algún tipo de metástasis coroidea. Así la presencia de ésta es sinónimo de enfermedad tardía y mal pronóstico
Manifestaciones clínicas
La coroides supone el destino del 88 % de los tumores uveales ( Shield, C; 1997) y de ellos entre 57 y 73 % serán postecuatoriales (Shield JA,) De ello se derivarán las manifestaciones clínicas de las metástasis coroideas: Visión borrosa, fotopsias, miodesopsias, metamorfopsias y ocasionalmente dolor.
En la exploración la masa coroidea puede sugerir la procedencia el tumor en base al color del mismo, así, una imagen color amarillento sugiere procedencia de pulmón, color anaranjado indicaría más probabilidad de origen reno-urotelial y color marronáceo en el caso de tumores melánicos metastásicos. Lo cual es importante, ya que hasta en el 34 % de los casos son la primera manifestación de la enfermedad tumoral aunque hasta en el 50 % de estos no se conocerá el origen primario. Fig 1
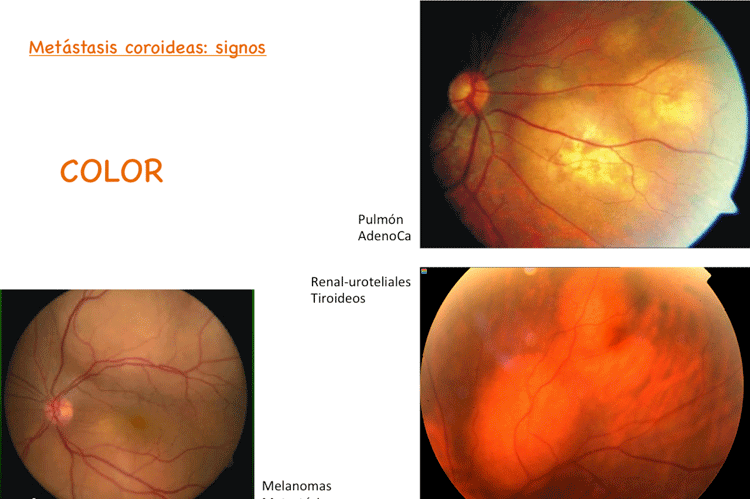
Figura 1. Diferentes colores en biomicroscopía de mtx coroideas
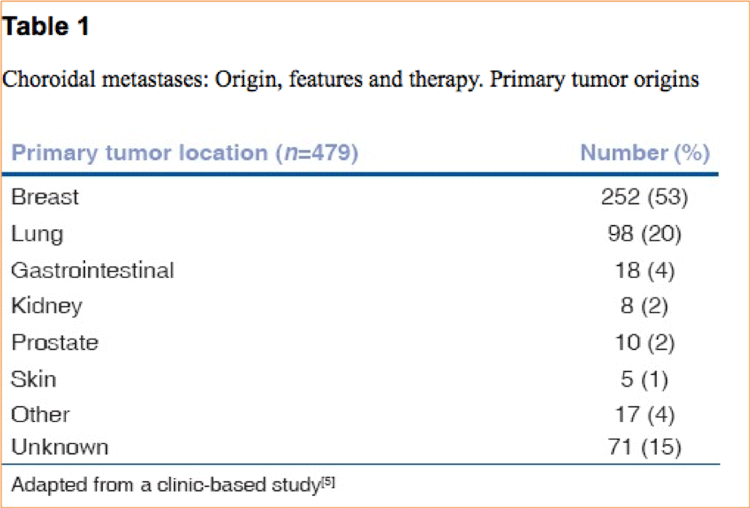
Figura 2. Origen de los tumores según. Indian J Ophthalmol. 2015 Feb; 63(2): 122127
En lo relativo a la localización, la mayor parte se localizarán en temporal (35%), seguido de superior (22%), inferior (17%), nasal ( 14%) y macular (12%).
Diagnóstico
La clave para el diagnóstico sigue siendo la ecografía, ya que lo localiza y define el tamaño. Nos dará múltiples ecos altos, irregulares y variables en función del origen, viendo en la ECO-B zonas silentes, correspondientes a necrosis lacunares (fig. 3). Frente a la imagen típica en ecos descendentes (Kappa) del melanoma (fig. 4) o los ecos altos regulares del hemangioma de coroides (fig. 5).

Figura 3. ECOS irregulares, altos, variables
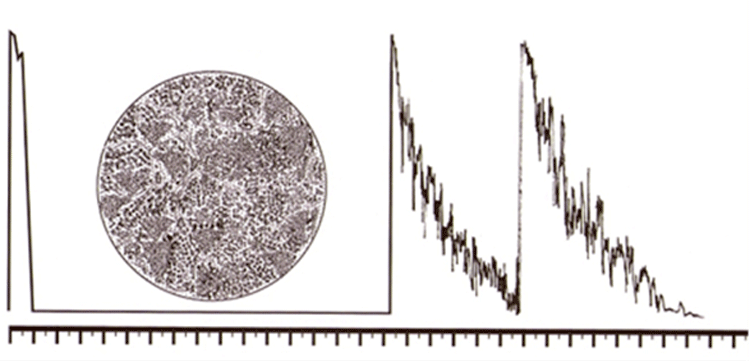
Figura 4. ECOs descendentes entre retina y esclera enmelanoma de coroides ( Ángulo Kappa)
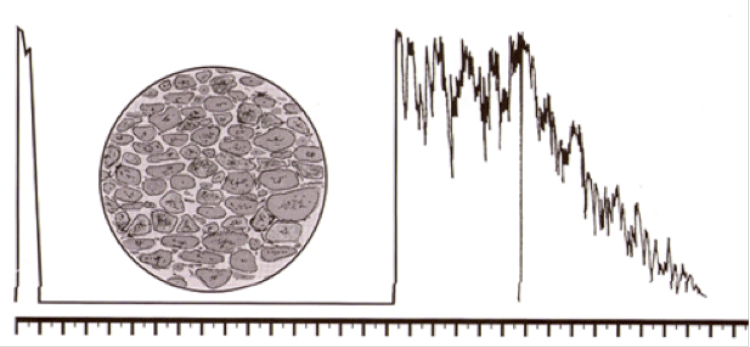
Figura 5. Hemangioma de coroides. Ecos altos regulares
No obstante, cada vez más, emplearemos las imágenes y los datos de la Tomografía de coherencia óptica ( OCT) para sumar criterios diagnósticos. Así, nos podemos encontrar un signo característico: Lumpy Grumpy, el EPR hace una línea ondulada, irregular con áreas de desprendimiento neurosensorial. Podemos encontrarnos puntos blancos y signos indirectos de inflamación intraestromal. En la imagen que la acompaña habitualmente, como es la infrarroja, aparecerá un punteado hiperrefectante irregular (fig. 6).
En la figura 7 resumimos el aspecto característico de la observación de OCT de los tumores coroideos, con la referencia del artículo que describe de manera muy esquemática y práctica (Say EA-2011)
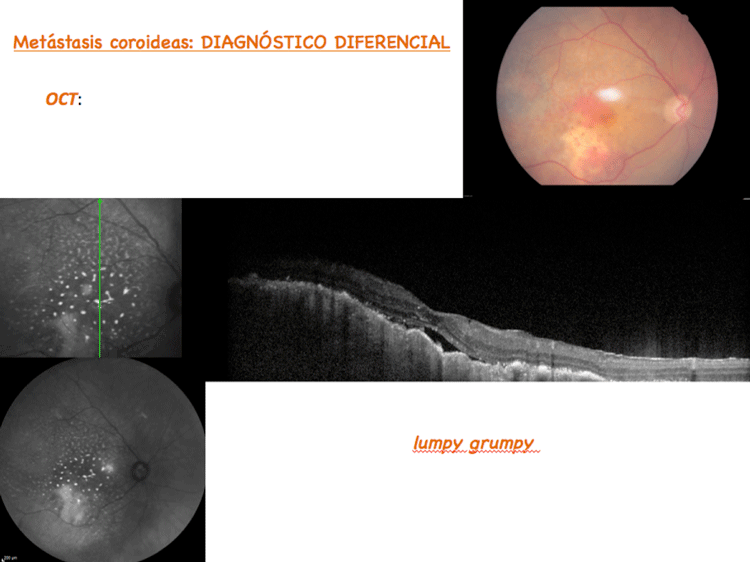
Figura 6. Retino y OCT característica de Mx coroidea
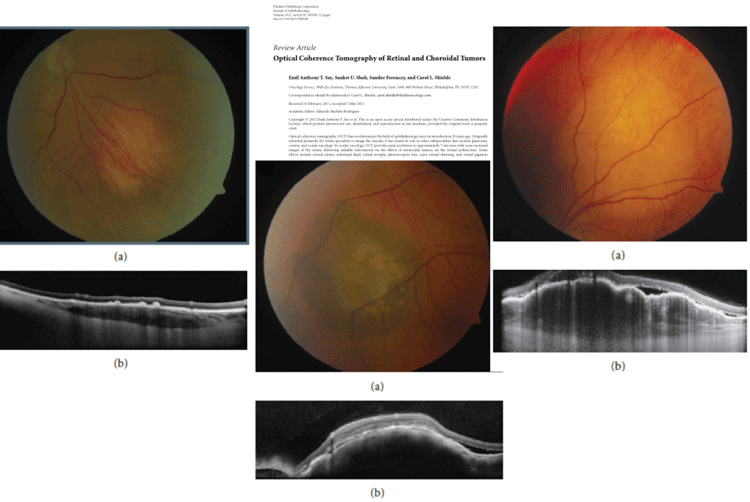
Fig 7: Referencia OCT de principales tumores coroideos
Otras herramientas que emplearemos puede ser la angiografía fluoresceínica, pero realmente tiene importancia relativa en el diagnóstico diferencial de las masas coroideas. <Ofrecen imágenes irregulares, con alta frecuencia de pin-points (73% de los casos) en la periferia de la lesión, pero estos hallazgos no son exclusivos. Igualmente la RMN no es determinante en el diagnóstico. Teóricamente nos ofrecerá imagen isointensa en T1 e hipointensa en T2, pero tampoco son diagnósticas 100%.
Las biopsias son necesarias en algunos casos, en los que se puede utilizar bien aspiración con aguja fina o extirpación biopsia mediante vitrectomo, cuando es necesario filiar el origen o en acasos de duda diagnóstica.
Tratamiento
Para el manejo de las metástasis hemos de considerar todas las opciones posibles, pero siempre condicionado al origen del tumor primario y la posible respuesta de éste al manejo sistémico, como es el caso de algunos tumores de mama con metástasis que pueden ser controlados con terapia hormonal.
Considerando metástasis únicas, con buen acceso, con pronóstico vital favorable, nos puede animar a estrategias como las de radioterapia ad-externo, con braquiterapia o como podemos ver desde algunas series antiguas (1977-ChuFC) con gamma Knife radiocirugía con protones; aunque son escasas las referencias.
Otras terapias como la antiangiogéncia, Fotodinámica, pueden ser de apoyo, pero poco resolutivas.
En casos de tamaño reducido y con posibilidades de preservación funcional, la extirpación directa puede ser una opción.
En un futuro inmediato, ya una realidad en algunos medios, la inmunoterpial con inhibidores del BRAF para melanomas y metástasis de éste (Ipilimumab, Nivolumab, ) nos abre otra puerta para la mejora de la calidad de vida de estos pacientes.