Evaluación de la resistencia mecánica de las esclerotomías en vitrectomía microincisional
López-Guajardo L1, Benítez-Herreros J2, Silva-Mato A3
1 Doctor en Medicina y Cirugía. Hospital Universitario Príncipe de Asturias (Alcalá de Henares, Madrid, España). Servicio de Oftalmología.
2 Licenciado en Medicina. Hospital Universitario Príncipe de Asturias (Alcalá de Henares, Madrid, España). Servicio de Oftalmología.
3 Profesor Titular Facultad de Medicina de la Universidad de Alcalá (Alcalá de Henares, Madrid, España). Dpto. CC. Sanitarias y Médico-Sociales
Resumen
Objetivos: Evaluar la resistencia mecánica de las esclerotomías oblicuas sin sutura en vitrectomía microincisional.
Métodos: Estudio experimental, prospectivo, aleatorizado y enmascarado. Practicamos vitrectomía sobre 120 ojos de cadáveres de cerdo enucleados. En sesenta ojos elegidos de forma aleatoria se realizaron esclerotomías oblicuas 23-gauge, para la entrada de la sonda de vitreotomía, y esclerotomías 25-gauge para el paso de la luz endocular. En los otros sesenta ojos se crearon incisiones oblicuas 25-gauge para el vitreotomo y 23-gauge para la luz. Al término de cada cirugía, retiramos las cánulas superiores e intercambiamos el suero intraocular por azul de metileno. A continuación elevamos la presión intraocular, monitorizada por el sistema de vitrectomía, hasta que alguna de las esclerotomías superiores mostró filtrado de líquido intraocular.
Resultados: Encontramos diferencias significativas entre el número de esclerotomías 23-gauge que drenaron líquido intraocular, con respecto de las incisiones 25-gauge. La presión a la que filtraron las esclerotomías 23-gauge fue significativamente menor que aquella a la que lo hicieron las incisiones 25-gauge. Por otro lado, no se observaron diferencias significativas entre la presión a la que filtraron las esclerotomías destinadas al paso del vitreotomo y a la sonda de iluminación.
Conclusiones: Las incisiones 23-gauge sin sutura presentan menor resistencia mecánica ante aumentos de la presión intraocular respecto de las esclerotomías 25-gauge. Por ello, la necesidad de emplear sutura al término de la cirugía será mayor en las esclerotomías 23-gauge que en las de 25-gauge.
Palabras clave: Resistencia mecánica, esclerotomía, oblicua, sin sutura, vitrectomía.
Abstract
Purpose: To determine the mechanical resistance of sutureless oblique sclerotomies in microincisional vitrectomy.
Methods: Experimental, prospective, randomized and observer-masked experimental study. In sixty randomized chosen eyes we performed 23-gauge oblique sclerotomies, for the entrance of the vitreous cutter probe, and 25-gauge oblique incisions for the endoillumination probe. In the other sixty eyes we created 25-gauge oblique sclerotomies for the vitreous cutter probe and 23-gauge oblique incisions for the endoillumination probe. At the end of the surgery, the superior cannulas were taken out of the eye and intraocular balanced salt solution was replaced with methylene blue. Then, intraocular pressure was elevated gradually by the vitrectomy system, until one of the superior sclerotomies became incompetent and showed leakage.
Results: The number of 23-gauge sclerotomies that showed leakeage was significantly higher than that of the 25-gauge. The pressure necessary to cause intraocular fluid leakage at the 23-gauge sclerotomies was significantly less than the pressure needed to cause incisional incompetency at the 25-gauge incisions. On the other hand, there were no statistically significant differences in the pressure necessary to cause intraocular leakage between the sclerotomies used by the vitreous cutter probe and the endoillumination probe.
Conclusions: Oblique 23-gauge sutureless sclerotomies offer less mechanical resistance to intraocular pressure rise than 25-gauge incisions in our experimental model. Surgeons should assume performing more sclerotomy suturing in 23-gauge cases to obtain similar closure standards.
Key Words: Mechanical resistance, sclerotomy, oblique, sutureless, vitrectomy.
Introducción
La vitrectomía transconjuntival sin sutura (VTS) se ha impuesto como técnica de primera elección en vitrectomía. Al eliminar la necesidad de suturas en las esclerotomías, se reduce la inflamación conjuntival postoperatoria, el astigmatismo inducido y el tiempo quirúrgico invertido en la apertura y cierre incisional.
El primero en describir la VTS fue Fujii (1,2), que realizó aperturas esclerales de 25-gauge perpendiculares a la esclera. Más adelante, en un intento por superar los inconvenientes que planteaba la flexibilidad del instrumental 25-gauge, Eckardt (3) introdujo el uso de material 23-gauge para la práctica de VTS.
Diversos estudios han evaluado la importancia del trayecto incisional en la creación de las esclerotomías, y cómo la dirección oblicua de estas parece mejorar su capacidad de cierre con respecto de las entradas directas (4-7).
En nuestro estudio, nos proponemos analizar la influencia que presentan el calibre de la esclerotomía (23 ó 25-gauge) y el uso al que esta se destine (paso de la sonda de vitrectomía o de la sonda de endoiluminación) en el comportamiento de las incisiones esclerales ante aumentos en la presión intraocular.
Material y métodos
Realizamos un estudio experimental, prospectivo, aleatorizado y con observador enmascarado, en el que seleccionamos 131 ojos procedentes de cerdos de la especie Sus scrofa domesticus, sacrificados para consumo humano una horas antes. Excluimos 11 por alteraciones conjuntivales, escleromalacia, opacidad de medios y desprendimiento de retina intraoperatorio.
En primer lugar, colocamos el ojo en un soporte que simula una órbita humana y que permite su fijación adecuada. A continuación, introducimos una aguja cerrada de 21-gauge por vía pars plana a las 6 h, que nos permitirá la práctica del experimento. Posteriormente, creamos la esclerotomía temporal inferior, por la cual introduciremos la línea de infusión. Para ello, desplazamos la conjuntiva con una pinza e insertamos el trocar de forma oblicua, describiendo un ángulo de 30° a 40° con la superficie escleral, paralelamente al limbo. Cuando la primera parte del trocar hubo entrado, rectificamos el ángulo hasta los 90° y metimos el resto del esclerotomo perpendicularmente a la superficie ocular. Por último, insertamos la vía de infusión de 23-gauge por dicha cánula.
A continuación, practicamos de la misma forma las esclerotomías superiores, destinadas al paso del vitreotomo y de la sonda de iluminación endocular, utilizando un trocar 23-gauge y otro 25-gauge en cada ojo alternativamente. Así, en 60 ojos elegidos de forma aleatoria, empleamos vitreotomo 23-gauge y luz 25-gauge, mientras que en otros 60 ojos utilizamos vitreotomo 25-gauge y luz 23-gauge. A continuación, aplicamos methocel® sobre la córnea y colocamos una lente de campo amplio (Volk®) sobre ésta.
Practicamos vitrectomía por vía pars plana de 23 ó 25-gauge según el caso, con el sistema de vitrectomía Accurus 800CS (Alcon Laboratories, Fort Worth, Texas, EEUU). Una vez completada la vitrectomía, retiramos las cánulas superiores, destapamos la aguja 21-gauge e intercambiamos la solución salina balanceada intraocular por azul de metileno 1%. Para ello, introducimos el colorante por la llave de tres pasos, hasta que refluyó por la aguja insertada a las 6 horas (fig. 1).
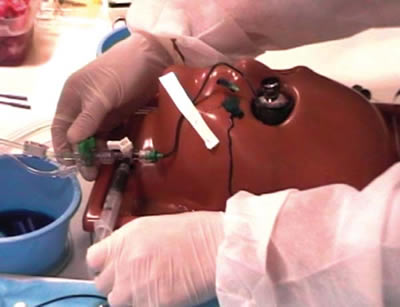
Fig. 1. Introducimos azul de metileno líquido 1% por la vía de infusión, a través de la llave de tres pasos, hasta que llenamos la cavidad vítrea y refluyó colorante por la aguja de 21-gauge introducida a las 6 horas.
Seguidamente bajamos la presión de infusión a 0 mm Hg, abrimos la entrada de solución salina a nivel de la llave de tres pasos, tapamos la aguja 21-gauge y elevamos la presión de infusión, monitorizada por el sistema de vitrectomía, hasta que un observador enmascarado observó filtrado de colorante a través de alguna de las esclerotomías superiores (fig. 2).
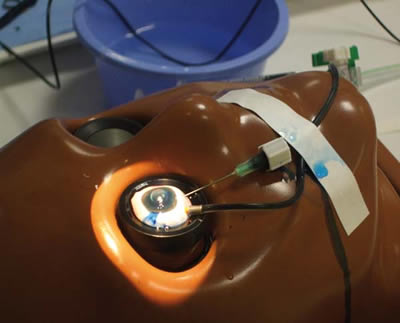
Fig. 2. Elevamos la presión intraocular hasta que una de las esclerotomías superiores mostró filtrado de azul de metileno.
En caso de llegar a los 120 mmHg que es la presión máxima que aplica el sistema, sin que se observe drenaje por parte de ninguna de las incisiones, aumentamos la presión digitalmente hasta que alguna de ellas cedió. Para ello, apretamos con los dedos índice a las 5 y a las 7 horas a nivel del limbo corneo-escleral, en dirección al centro del ojo. En estos casos, la presión intraocular registrada fue de > 120 mmHg. Finalmente, incluimos en una base de datos todos los resultados obtenidos.
Resultados
Encontramos diferencias significativas entre el número de esclerotomías 23-gauge que drenaron líquido intraocular, con respecto de las incisiones 25-gauge que mostraron esta incompetencia (P = 0,02, test de una proporción) (fig. 3). Al analizar de forma cuantitativa las presiones de infusión a las que filtraron las esclerotomías en función de su calibre, también existieron diferencias significativas, de forma que las entradas 23-gauge mostraron filtrado a presiones significativamente menores (P < 0,0001, test de los rangos de Wilcoxon).
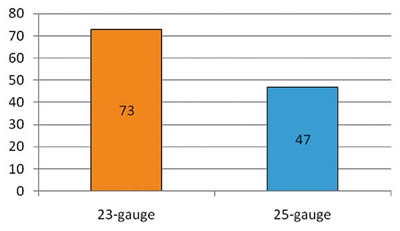
Fig. 3. Diagrama de barras. Número de esclerotomías que mostraron drenaje de líquido en función de su calibre.
Por otro lado, no hallamos diferencias significativas entre el número de esclerotomías destinadas al paso de la sonda del vitreotomo que drenaron líquido intraocular, con respecto de las incisiones usadas por la sonda de iluminación que mostraron esta incompetencia (P = 0,58, test de una proporción) (fig. 4). Tampoco encontramos diferencias al estudiar las presiones de infusión a las que filtraron líquido las esclerotomías en función de uso (P = 0,77, test de los rangos de Wilcoxon).
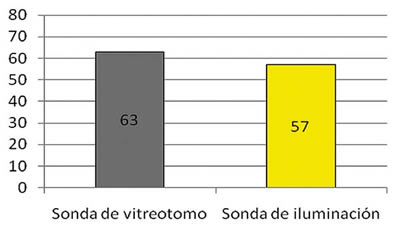
Fig. 4. Diagrama de barras. Número de esclerotomías que mostraron drenaje de líquido en función del uso al que estuvieran destinadas.
Conclusiones
Para la realización de nuestro estudio, elaboramos un modelo experimental animal que simulara en lo posible las condiciones encontradas en la práctica habitual de vitrectomía. Para ello, empleamos material y tecnología idénticos a los utilizados en los procedimientos quirúrgicos reales sobre humanos, además de ojos de cerdo de la especie Sus scrofa domesticus. La facilidad que supone la obtención de un gran número de estos ojos, y las similitudes que presentan con los ojos humanos (8,9), justificaron nuestra elección.
De nuestra experiencia se extrae que el diferente diámetro de las incisiones 23 y 25-gauge oblicuas, influye de forma significativa en la capacidad de cierre escleral, siendo este más eficaz en las entradas 25-gauge oblicuas. Nuestros resultados son acordes con la tendencia general observada por diversos estudios observacionales, que revelan mayor necesidad de sutura (10,11) y mayores tasas de hipotonía (10,11) tras vitrectomía a través de incisiones oblicuas 23-gauge, con respecto de la mostrada por otros trabajos que analizan estos parámetros después de vitrectomía mediante esclerotomías oblicuas 25-gauge (7).
En nuestro estudio, analizamos la resistencia mecánica de las incisiones esclerales ante aumentos de presión intraocular, en ausencia de mecanismos de reparación tisular. Por ello, el periodo durante el cual nuestros resultados se pueden aplicar en la práctica clínica habitual, se sitúa entre la retirada de las cánulas, y el cierre escleral por proliferación tisular, que estudios experimentales en animales establecen entre el segundo y el quinto día tras la intervención (12,13), y trabajos en humanos con biomicroscopía ultrasónica sitúan entre el séptimo y el quinceavo día tras la práctica de las esclerotomías (6,14).
El hecho de que nuestro estudio sea aplicable solo durante los primeros días tras la cirugía no le resta importancia clínica, ya que los primeros signos clínicos de endoftalmtis postquirúrgica aguda suelen aparecer, como media, en el tercer día tras la cirugía (15,16). Esto significa que la contaminación bacteriana puede darse durante la cirugía o en los primeros días tras la intervención, cuando el cierre escleral depende principalmente de factores mecánicos. Por tanto, la capacidad de cierre de las esclerotomías en el postoperatorio inmediato tras una vitrectomía, se antoja de gran importancia a la hora de mantener el ojo libre de infecciones intraoculares.
Al analizar los datos recogidos, no encontramos diferencias estadísticamente significativas entre el número de esclerotomías oblicuas utilizadas por la sonda de vitrectomía, manejada por la mano dominante, y el número de incisiones oblicuas empleadas por la sonda de iluminación, manipulada por la mano no dominante, que drenaron líquido intraocular en primer lugar. Por ello, el paso de la sonda del vitreotomo o de la luz, así como las diferentes maniobras que implica el manejo de cada una, no influyen significativamente en la capacidad de cierre incisional.
Bibliografía
- Fujii GY, de Juan E Jr, Humayun MS, et al. A new 25-gauge instrument system for transconjunctival sutureless vitrectomy surgery. Ophthalmolgy 2002; 109: 1807-13.
- Fujii GY, de Juan Ejr, Humayun MS, et al. Initial experience using the transconjunctival sutureless vitrectomy system for vitreoretina surgery. Ophthalmology 2002; 109: 1814-20.
- Eckardt C. Transconjunctival sutureless 23-gauge vitrectomy. Retina 2005; 25: 208-11.
- López-Guajardo L, Pareja-Esteban J, Teus-Guezala MA. Oblique sclerotomy technique for prevention of incompetent wound closure in transconjunctival 25-gauge vitrectomy. Am J Ophthalmol 2006; 141: 1154-6.
- Shimada H, Nakashizuka H, Mori R, Mizutani Y, Hattori T. 25-gauge scleral tunnel transconjunctival vitrectomy. Am J Ophthalmol 2006; 142: 871-3.
- López-Guajardo L, Vleming-Pinilla E, Pareja-Esteban J, Teus-Guezala MA. Ultrasound biomicroscopy study of direct and oblique 25-gauge vitrectomy sclerotomies. Am J Ophthalmol 2007; 143: 881-3.
- Hsu J, Chen E, Gupta O, Fineman MS, Garg SJ, Regillo CD. Hypotony after 25-gauge vitrectomy using oblique versus direct cannula insertions in fluid-filled eyes. Retina 2008; 28: 937-40.
- Olsen TW, Sanderson S, Feng X, Hubbard WC. Porcine sclera: thickness and surface area. Invest Ophthalmol Vis Sci 2002; 43: 2529-32.
- Nicoli S, Ferrari G, Quarta M, Macaluso C, Govoni P, Dallatana D, Santi P. Porcine sclera as a model of human sclera for in vitro transport experiments: histology, SEM, and comparative permeability. Mol Vis 2009; 15: 259-66.
- Parolini B, Prigione G, Romanelli F, Cereda MG, Sartore M, Pertile G.Postoperative complications and intraocular pressure in 943 consecutive cases of 23-gauge transconjunctival pars plana vitrectomy with 1-year follow-up. Retina. 2010; 30: 107-11.
- Woo SJ, Park KH, Hwang JM, Kim JH, Yu YS, Chung H. Risk factors associated with sclerotomy leakage and postoperative hypotony after 23-gauge transconjunctival sutureless vitrectomy. Retina 2009; 29: 456-63.
- Zhengyu S, Fang W, Ying F, Qinghua Q. The experimental research of rabbit’s sclerotomy sites undergoing transconjunctival sutureless vitrectomy. Curr Eye Res 2007; 32: 647-52.
- Hikichi T, Yoshida A, Hasegawa T, Ohnishi M, Sato T, Muraoka S. Wound healing of scleral self-sealing incision: a comparison of ultrasound biomicroscopy and histology findings. Graefe’s Arch Clin Exp Ophthalmol 1998; 236: 775-8.
- Rizzo S, Genovesi-Ebert F, Vento A, Miniaci S, Cresti F, Palla M. Modified incision in 25-gauge vitrectomy in the creation of a tunneled airtight sclerotomy: an ultrabiomicroscopic study. Graefes Arch Clin Exp Ophthalmol 2007; 245: 1281-8.
- Kunimoto DY, Kaiser RS. Incidence of endophthalmitis after 20- and 25-gauge vitrectomy. Ophthalmology 2007; 114: 2133-37.
- Scott IU, Flynn HW Jr, Dev S, Shaikh S, Mittra RA, Arevalo JF, Kychenthal A, Acar N. Endophthalmitis after 25-gauge and 20-gauge pars plana vitrectomy: incidence and outcomes. Retina 2008; 28: 138-4.